INTRODUÇÃO:
A síndrome antifosfolípidica (SAF) é uma doença auto-imune sistémica caraterizada por trombose vascular e/ou morbilidade gestacional, associada à persistência de anticorpos anti-fosfolipídicos1(aPL). Estima-se que afete cerca de 40 a 50 indivíduos por cada 100.000 habitantes na população geral1. Embora possa ocorrer na sua forma primária (ou idiopática), em alguns casos a SAF surge como secundária a outras doenças, tais como o lúpus eritematoso sistémico ou as neoplasias4.
As doenças linfoproliferativas (DLP), por sua vez, podem-se associar a fenómenos imunológicos, estimando-se que entre 26 a 35% dos doentes com linfoma apresentem positividade para os aPL2,8. Ainda permanece por esclarecer se a positividade destes últimos é apenas um epifenómeno das neoplasias ou se, por outro lado, contribuem ativamente para o desenvolvimento de fenómenos trombóticos nestes doentes3.
O anticoagulante lúpico (ACL) parece ser o aPL que confere maior risco trombótico3e o que mais frequentemente se encontra positivo nas doenças linfoproliferativas. Inclusivamente, alguns estudos apontam que a presença de aPL permite identificar os doentes com maior risco trombótico, assim como avaliar a resposta à terapêutica e prever a recidiva das DLP e a sobrevida4,9.
Pela sua multiplicidade de manifestações, algumas delas inespecíficas, o diagnóstico das doenças linfoproliferativas, e em particular do linfoma de Hodgkin poderá constituir um desafio, principalmente quando associado a outras entidades clínicas, cuja correlação fisiopatológica ainda não está bem esclarecida, como é o caso da síndrome antifosfolípidica.
CASO CLÍNICO:
Descreve-se o caso de um homem com 57 anos, autónomo, leucodérmico, casado e que trabalhava como vendedor. Apresentava como antecedentes patológicos: hipertensão arterial essencial e dislipidemia medicadas com losartan 50mg/dia e sinvastatina 20mg/dia, respetivamente. Sem história familiar relevante.
Em fevereiro de 2017 foi diagnosticado com trombose venosa profunda do membro inferior direito. Iniciou anticoagulação com rivaroxabano 20mg/dia e foi seguido em consulta de Imunohemoterapia durante seis meses. Após este período suspendeu o fármaco, e duas semanas depois colheu estudo analítico com doseamento de anticorpos antifosfolipídicos, mas faltou à consulta de reavaliação e perdeu o seguimento. Em março de 2018 recorreu ao serviço de urgência por amaurose de instalação súbita, tendo sido diagnosticada trombose arterial da retina do olho direito. A angiografia do olho direito mostrou esclerose arterial com atraso no preenchimento vascular. Iniciou anti-agregação e foi referenciado a consulta de Medicina Interna para estudo de causas pró-trombóticas.
Na anamnese realizada na consulta de Medicina Interna destacava-se a referência a lombalgia de ritmo misto com vários anos de evolução, sem agravamento recente e a ausência de outra sintomatologia associada, nomeadamente sintomas constitucionais. No exame objetivo salientava-se a identificação de um nódulo cervical esquerdo com cerca de 2cm de maior eixo, mole, pouco móvel e indolor, e a presença de lesões cutâneas eritematosas, sem relevo, arredondadas, não pruriginosas e indolores na face anterior de ambos os membros inferiores. Não foram identificadas outras alterações relevantes ao exame físico.
Na revisão do processo clínico foi constatada a positividade do anticoagulante lúpico no estudo analítico realizado em setembro de 2017.
Do estudo laboratorial realizado na consulta de Medicina Interna destacava-se a presença de anemia normocromica, normocítica, elevação da velocidade de sedimentação e da proteína C reativa (tabela 1), com lactato desidrogenase e parâmetros referentes à função renal e hepática normais. O doseamento de anticoagulante lúpico (intervalado por mais de 12 semanas em relação ao previamente conhecido) foi positivo, sendo os anticorpos anticardiolipina (IgG e IgM) e B2-glicoproteína (IgG e IgM) negativos. A restante investigação de auto-imunidade e serologias víricas foi negativa.
Portanto, foi estabelecido o diagnóstico de síndrome antifosfolípidica e o doente iniciou anticoagulação com varfarina.
Foi realizada biopsia de uma das lesões cutâneas, cujo exame histológico mostrou fenómenos de vasculite linfocítica (figura 1).
Na pesquisa de eventuais causas secundárias associadas à SAF, o doente realizou telerradiografia torácica que mostrou alargamento do mediastino com contornos lobulados (figura 2). A tomografia computorizada cervico-toraco-abdomino-pélvica confirmou a presença de adenomegalias mediastínicas e abdominais, com descrição de extensa trombose da veia cava inferior com transformação cavernomatosa (figura 3). O fígado e baço eram normais. Pelas queixas de lombalgia crónica realizou, ainda, tomografia computorizada da coluna e, posteriormente, ressonância magnética que descrevia lesões líticas em L4, L5 e S1, com fratura patológica a nível de L4 (figura 4).
Perante a suspeita de doença neoplásica associada, possivelmente linfoproliferativa, foi alargado o estudo complementar e o doente realizou uma tomografia por emissão de positrões que confirmou a presença de várias adenopatias hipermetabólicas a nível mediastínico, cervical, supra-clavicular e abdominal e de lesões líticas ósseas com idêntico padrão de captação do radiofármaco, sugerindo doença de etiologia comum (figura 5).
Foi realizada biopsia excisional de gânglio cervical, cujo exame anátomo-patológico revelou tratar-se de linfoma de Hodgkin na variante de esclerose nodular em estadio IV pela classificação de Lungano.
Consequentemente, a estratégia de anticoagulação foi alterada para enoxaparina na dose de 1.5mg/kg/dia e o doente foi rapidamente referenciado a consulta de Hematologia e de Ortopedia. Dada a estabilidade da fratura de L4, teve apenas indicação para uso de lombostato e analgesia. Cumpriu 6 ciclos de ABVD (adriamicina, bleomicina, vinblastina e dacarbazina) sem intercorrências, atingindo a remissão completa da doença em Abril de 2019.
Cerca de 3 meses pós o término da quimioterapia, o doente mantem-se livre de doença neoplásica, encontrando-se em seguimento em consulta de Hematologia, Ortopedia e Medicina Interna Doenças auto-imunes.
DISCUSSÃO:
As doenças linfoproliferativas, e em particular o linfoma de Hodgkin, correspondem a cerca de 0.5% de novos casos de cancro nos Estados Unidos. Os achados mais comuns são as adenopatias, principalmente mediastínicas e os sintomas B acompanhantes9. Em casos mais avançados pode ocorrer atingimento extra-ganglionar, sendo o pulmão, fígado e osso os órgãos habitualmente afetados. Embora seja considerado raro, o Linfoma de Hodgkin pode-se associar a condições auto-imunes, como vasculites ou síndromes trombóticas para-neoplásicas10.
A positividade dos aPL, como é o caso do anticoagulante lúpico, nas doenças linfoproliferativas tem vindo a ser um achado cada vez mais descrito na literatura, embora sejam ainda imprecisas as suas implicações na trombose associada ao cancro.
No caso concreto desde doente salienta-se três aspetos atípicos na apresentação do Linfoma de Hodgkin: 1) a ausência de sintomas B (habitualmente presentes em mais de 90% dos casos, em particular na doença avançada) e a normalidade de marcadores como a lactato desidrogenase e a beta2 microglobulina; 2) o envolvimento extra-ganglionar com atingimento ósseo na forma de lesões líticas, podendo mimetizar outras entidades nosológicas; 3) a síndrome antifosfolípidica como manifestação inaugural da doença, correspondendo provavelmente à sua forma secundária.
De uma forma geral, este caso procura enfatizar a importância de exclusão de causas secundárias da SAF, nomeadamente as de etiologia hemato-oncológica.
Em conclusão, está atualmente bem fundamentado na literatura que a SAF e as doenças linfoproliferativas constituem entidades promotoras de eventos trombóticos. Embora pareça existir uma correlação entre ambas, principalmente a positividade do ACL, o mecanismo fisiopatológico específico que as liga permanece ainda por esclarecer. No futuro o conhecimento mais alargado sobre estas duas entidades e a sua relação poderá contribuir para uma melhor estratificação do risco trombótico de grupos particulares de doentes, minimizando a morbilidade associada a estas duas patologias.
Quadro I
Estudo laboratorial realizado durante a investigação na consulta de Medicina Interna.
| | | | |
| Parâmetro | Valor obtido (valores de referência) | Parâmetro | Valor obtido (valores de referência) |
| Hemoglobina (g/dl) | 9,8 (13.5-17.5) | Enzima de Conversão da Angiotensina (U/L) | 64 (35-90) |
| Leucócitos (x109/L) | 4,2 (4.5-11.0) | Anticorpos anti-nucleares | negativo |
| Linfócitos (%) | 18% (25-33%) | Anticorpos Anti-DNA | negativo |
| Velocidade de Sedimentação (mm/1h) | >120 (0-15) | Anticoagulante Lúpico | positivo |
| Proteína C Reativa (mg/L) | 185 (0-5) | Anticorpos Anti-Cardiolipina | negativo |
| Sedimento Urinário | normal | Anticorpos Anti-B2 Glicoproteina | negativo |
| Lactato Desidrogenase (U/L) | 200 (120-240) | Imunoglobulinas A, M, G | normais |
| Vírus de imunodeficiência humana | negativo | Eletroforese sérica e Urinária | normais |
| Vírus da Hepatite C e B | negativo | B2 microglobulina (mg/ml) | 1.2 (<2) |
Tabela 1. Principais resultados analíticos do estudo complementar realizado.
Figura I
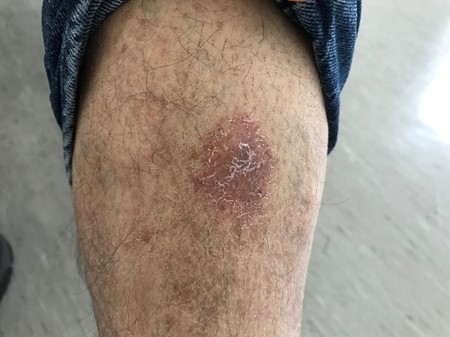
Lesão eritematosa de limites definidos, sem relevo, indolor e não pruriginosa, na face anterior da perna esquerda.
Figura II
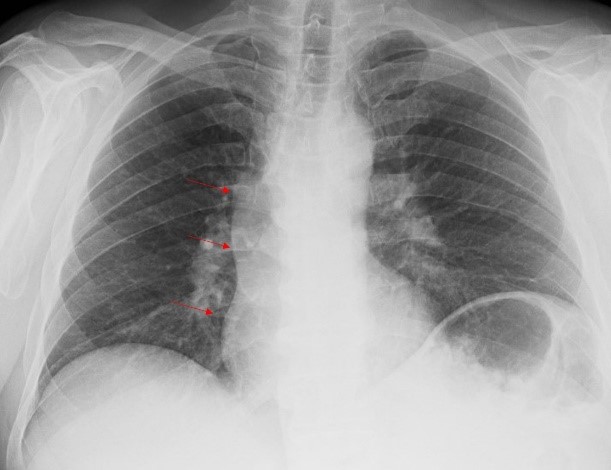
Telerradiografia torácica a mostrar alargamento do mediastino com contornos lobulados (setas vermelhas).
Figura III
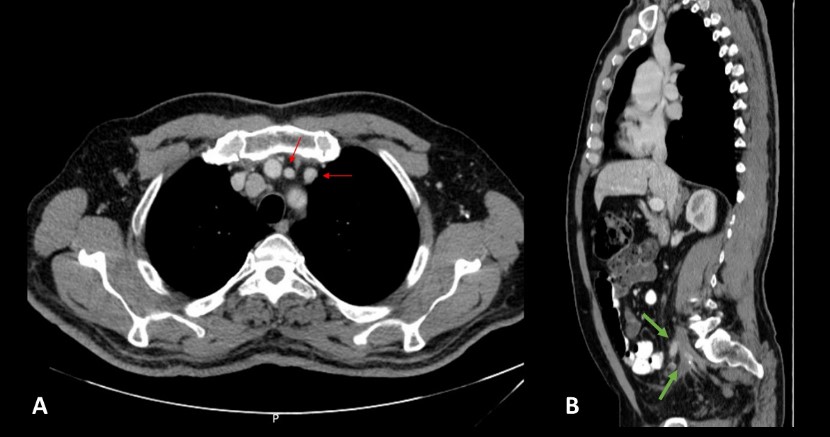
Tomografia computorizada do tórax (A) a mostrar adenopatias mediastínicas (setas vermelhas) e abdomino-pélvica (B) com identificação de trombose da veia cava inferior com transformação cavernomatosa (setas verdes).
Figura IV
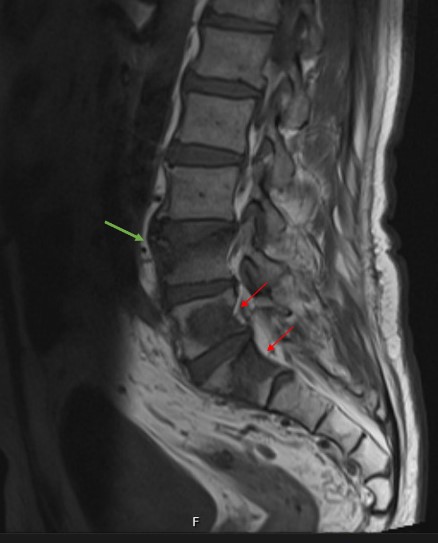
Ressonância Magnética da coluna lombossagrada, com ponderação em T2, a mostrar lesões líticas em L5 e S1 (setas vermelhas) e a fratura patológica a nível de L4 (seta verde).
Figura V
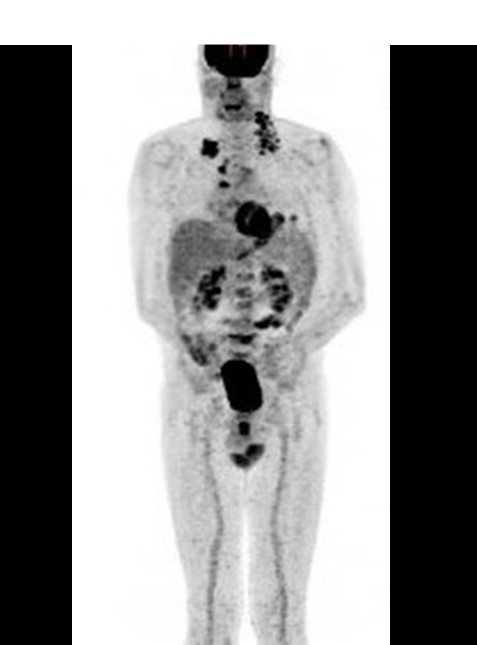
Tomografia de Emissão de Positrões a mostrar a infiltração ganglionar acima e abaixo do diafragma e a nível ósseo antes do tratamento.
BIBLIOGRAFIA
1. Mezhov V, Segan J, Tran H, et al. Antiphospholipid syndrome: a clinical review. Med J Aust. 2019. 211(4):184-188;
2. Genvresse I, Luftner D, Buttgereit F, et al. Prevalence and clinical significance of anticardiolipin and anti-B2-glycoprotein-I antibodies in patients with non-Hodgkins lymphoma, Eur J Haematol. 2002. 68(2):84-90;
3. Miesbach W, Scharrer I, Asherson A. High titres of IgM-antiphospholipid antibodies are unrelated to pathogenicity in patients with non-Hodgkins lymphoma. Clin Rheumatol. 2007. 26(1):95-7;
4. Lilangi S, Ediriwickrema MS, Zaheer MD. Diffuse large cell lymphoma presenting as sacral mass and lupus anticoagulant. Yale J Biol Med. 2011. 84(4): 433438;
5. Miesbach W, Scharrer I, Asherson A. Thrombotic manifestations of the antiphospholipid syndrome in patients with malignancies. Clin Rheumatol. 2006. 25(6):840-4;
6. Wilde C, Herregods MC, Verhoef G et al. A patient with hodgkins lymphoma, antiphospholipid syndrome and severe mitral insuffiency. Acta Clin Belg. 2006.61(4):183-7;
7. McGuire D, Zeidman A, Mittelman M. Non-Hodgkins lymphoma presenting with coagulopathy due to antiphospholipid antibody syndrome. Leuk Lymphoma. 1997. 26(1-2):193-6;
8. Stari R, Stipa E, Masi M et al. Antiphospholipid antibodies: prevalence, clinical significance and correlation to cytokine levels in acute myeloid leukemia and a non-Hodgkins lymphoma. Thromb Haemost. 1993. 70(4):568-72.
9. Shanbhag S, Ambinder R. Hodgkin Lymphoma: a review and update on recent progress. CA Cancer J Clin. 2018. 68(2):116-132;
10. Connors JM. Clinical Manifestations and Natural History of Hodgkins Lymphoma. Cancer J. 2009. 15(2):124-8.






