INTRODUÇÃO
As EPP são um grupo de patologias raras, caracterizadas pela perda proteica excessiva a nível do trato digestivo. Condicionam hipoproteinémia, edemas e maior predisposição para infeções, na ausência de proteinúria ou defeitos na síntese proteica (como em casos de malnutrição ou patologia hepática crónica).1,3
As EPP podem ser consequência de obstrução linfática, patologias gástricas, intestinais ou cardíacas.1 A PC representa uma etiologia incomum desta patologia. Esta corresponde ao derradeiro estágio de um processo inflamatório crónico e que é responsável pelo encarceramento das cavidades cardíacas, com prejuízo do enchimento diastólico ventricular, aumento da pressão venosa a montante, condicionamento da drenagem linfática intestinal, com consequente perda proteica.4,5
CASO CLÍNICO
Um homem de 54 anos com antecedentes pessoais de hipertensão arterial, asma brônquica, insuficiência venosa, erisipelas de repetição desde há 6 meses e tuberculose pulmonar e intestinal aos 18 anos, foi ao Serviço de Urgência, no contexto de erisipela do membro inferior direito e edemas generalizados. Negava dispneia, ortopneia, dispneia paroxística noturna, diarreia, viagens recentes ou realização de antibioterapia no mês prévio.
Ao exame objetivo apresentava-se apirético, hemodinamicamente estável; sem sinais de desnutrição, sinal de Kussmaul negativo, auscultação cardíaca com sons cardíacos rítmicos e regulares, sem sopros, extra-sons ou atrito pericárdico; auscultação pulmonar com murmúrio vesicular mantido, sem ruídos adventícios. Não foi avaliada a presença de pulso paradoxal. Revelava marcado edema da parede abdominal e membros inferiores, com sinais inflamatórios exuberantes no membro inferior direito até à coxa.
O electrocardiograma à admissão encontrava-se em ritmo sinusal, apresentando baixa voltagem.
Analiticamente, o doente apresentava elevação dos parâmetros inflamatórios (com leucocitose, neutrofilia e linfopenia), função hepática e renal normais, tendo sido internado para estudo e terapêutica.
No decurso da investigação etiológica, apresentava níveis de coagulação normais (tempo de protrombina 10.9s, tempo de tromboplastina parcial ativada 27s), ausência de proteinúria significativa (150mg em 24h), peptídeo natriurético do tipo B (BNP) de 84pg/mL, colesterol total de 143mg/dL, HDL 22 mg/dL, LDL 87.6 mg/dL e triglicerídeos 167 mg/dL, bem como anticorpos anti-transglutaminase e anti-gliadina normais.
Apresentava, no entanto, défice de proteínas totais (37.1 g/L), hipoalbuminémia (18.5 g/L), défice de IgA e IgG, com IgM normal, défice funcional de ferro, bem como hiperparatiroidismo secundário a défice de vitamina D.
Realizou estudo das fezes que revelou um aumento da alfa-1 antitripsina, sugerindo EPP. Foram então realizadas uma Endoscopia Digestiva Alta (EDA), uma Coloscopia, uma Tomografia Computadorizada (TC) e um Ecocardiograma Transtorácico (ETT) para estudo etiológico.
A EDA revelou linfangiectasias na segunda porção do duodeno, sem aparente atrofia das vilosidades a nível macroscópico (Figura 1). Realizou biópsia duodenal que revelou ligeiro achatamento de algumas vilosidades, sem aumento significativo da permeação do epitélio entérico por linfócitos, raras linfangiectasias com alguns eosinófilos e raros linfócitos. A Colonoscopia não revelou alterações significativas.
A TC tóraco-abdominal mostrou espessamento pericárdio difuso com áreas de calcificação em placa, compatível com PC (Figuras 2, 3 e 4). No entanto, após o internamento, foram realizados dois ETT no espaço de 4 meses, não tendo sido confirmado o diagnóstico de PC.
Posteriormente, realizou uma Vídeocapsula Entérica, sendo observável marcado edema na mucosa jejunal e duodenal, com coalescência de vilosidades edematosas; no jejuno médio o edema era menos acentuado; área congestiva no cólon direito. Todos estes aspetos sugeriam uma enteropatia congestiva.
Nos 2 anos seguintes, o doente apresentou quatro novos episódios de erisipela (três com necessidade de hospitalização) e dois outros internamentos por agravamento dos edemas, necessitando de reposição de albumina. Durante este período desenvolveu ainda uma fibrilhação auricular permanente.
Na última hospitalização, foi novamente realizado um ETT (Figuras 5), que indicava um ventrículo esquerdo não dilatado, alongado com ressalto do septo interventricular e interdependência ventricular, variação de fluxos transmitral e tricúspide sugestivos de constrição ao enchimento, dilatação bi-auricular e plétora da veia cava inferior com cinética respiratória ausente. Estes achados corroboravam o diagnóstico de PC.
Foram realizados angiografia coronária diagnóstica e estudo hemodinâmico, que revelaram equalização das pressões telediastólicas em todas as cavidades cardíacas, confirmando a constrição (Figura 6).
O caso foi então encaminhado para a cirurgia cardiotorácica que realizou uma pericardiectomia. Não foi, contudo, realizada Ressonância Magnética Cardíaca antes do procedimento. Na mesa operatória, o pericárdio apresentava espessamento e múltiplas placas calcificadas, principalmente na metade direita do coração, causando constrição severa das cavidades direitas. A peça cirúrgica acabou por não ser enviada para a anatomia patológica, não tendo por isso sido realizada pesquisa de DNA de Mycobacterium tuberculosis na mesma.
O doente encontra-se atualmente medicado com lisinopril 5mg, torasemida 5mg, rivaroxabano 20mg, lanoxin 0.125mg e colecalciferol. Desde a pericardiectomia, realizada há 5 anos, verificou-se uma franca melhoria da sua qualidade de vida, sem quaisquer edemas ou novos episódios de erisipela. Os valores de proteínas totais e albumina normalizaram (74.8 g/L e 47.5 g/L respetivamente, nas últimas análises).
DISCUSSÃO
O diagnóstico de EPP é sugerido pela presença de edema e hipoproteinémia, na ausência de desnutrição, insuficiência hepática ou síndrome nefrótico. 1,3 Após a exclusão destas últimas, os valores de alfa1-antitripsina nas fezes são um bom indicador das perdas gastrointestinais, uma vez que esta proteína normalmente não é absorvida ou secretada no intestino1.
As perdas proteicas a nível gastrointestinal podem ser resultado de lesão da mucosa ou de disfunção linfática. Esta última pode ser primária ou secundária a uma obstrução, nomeadamente por patologia cardíaca.3
Quando a alfa1-antitripsina fecal se encontra aumentada, a realização da EDA, da TC tóraco-abdominal e do ETT são então mandatórios, no sentido de se excluir etiologias digestiva, linfática ou cardíaca.1
A PC é uma das causas cardíacas das EPP. É o estágio final de um processo inflamatório crónico, que ocorre pela formação de tecido de granulação e obliteração da cavidade pericárdica.4 Pode existir calcificação pericárdica, sendo esta mais comum na pericardite tuberculosa.3,6
O encarceramento das câmaras cardíacas pela fibrose e calcificação do pericárdio prejudica o enchimento diastólico ventricular, aumenta a pressão venosa a montante, afetando a normal drenagem linfática intestinal, condicionando a perda proteica.4,5 A hipoalbuminémia resultante dessas perdas causa uma diminuição da pressão oncótica plasmática, levando ao edema.7
Para além das perdas de albumina, existem ainda perdas significativas de imunoglobulinas e linfócitos, que predispuseram o paciente a infeções de repetição (neste caso a erisipelas).1
O ETT é relevante no diagnóstico de PC, bem como para o diagnóstico diferencial com outras causas de disfunção ventricular direita.5
Nesse sentido, é importante a distinção com a cardiomiopatia restritiva, atendendo a que apresentam algumas semelhanças (apresentação clínica insidiosa, restrição ao enchimento ventricular) mas fisiopatologia e orientações terapêuticas distintas.6
Na PC, ao contrário da miocardiopatia restritiva, o ETT pode apresentar espessamento pericárdico e calcificações, deslocamento do septo durante o ciclo respiratório, causada pela variabilidade no retorno venoso e interdependência ventricular.5,6
No entanto, o ETT não permite estabelecer ou excluir definitivamente o diagnóstico, sendo para isso úteis a TC e a Ressonância Magnética.3 O gold standart para a confirmação do diagnóstico é o cateterismo cardíaco, com análise das curvas de pressão intracavitárias. Estas estão classicamente elevadas, com equalização telediastólica das pressões em todas as cavidades.5,6 Como resultado das limitações impostas por um pericárdio rígido e espessado, o enchimento ventricular diastólico está comprometido, assemelhando-se o traçado da pressão ventricular ao sinal da raiz quadrada (“dip plateau”), com enchimento diastólico precoce rápido, seguido de estabilização da pressão ventricular.3
CONCLUSÃO
A PC representa uma causa incomum de EPP. O encarceramento das câmaras cardíacas por um pericárdio rígido e espessado é responsável pelo aumento da pressão venosa a montante, limitando a drenagem linfática intestinal. Esta limitação conduz a hipoproteinémia e perda de imunoglobulinas e linfócitos, originando edemas e infeções de repetição.
Uma vez resolvida a constrição, através de uma pericardiectomia, as pressões venosas e drenagem linfática normalizaram, com resolução da hipoproteinémia, edemas e intercorrências infeciosas.
Para concluir, importa salientar que quaisquer exames complementares de diagnóstico podem representar falsos negativos e nos desviar do diagnóstico correto. Neste caso, e no contexto de uma EPP de etiologia cardíaca, o ETT é um método diagnóstico fundamental, mas apenas demonstra sinais óbvios de constrição em cerca de 50 a 70% dos casos.8 Com vista ao melhor interesse do doente, o julgamento clínico deve prevalecer.
Figura I
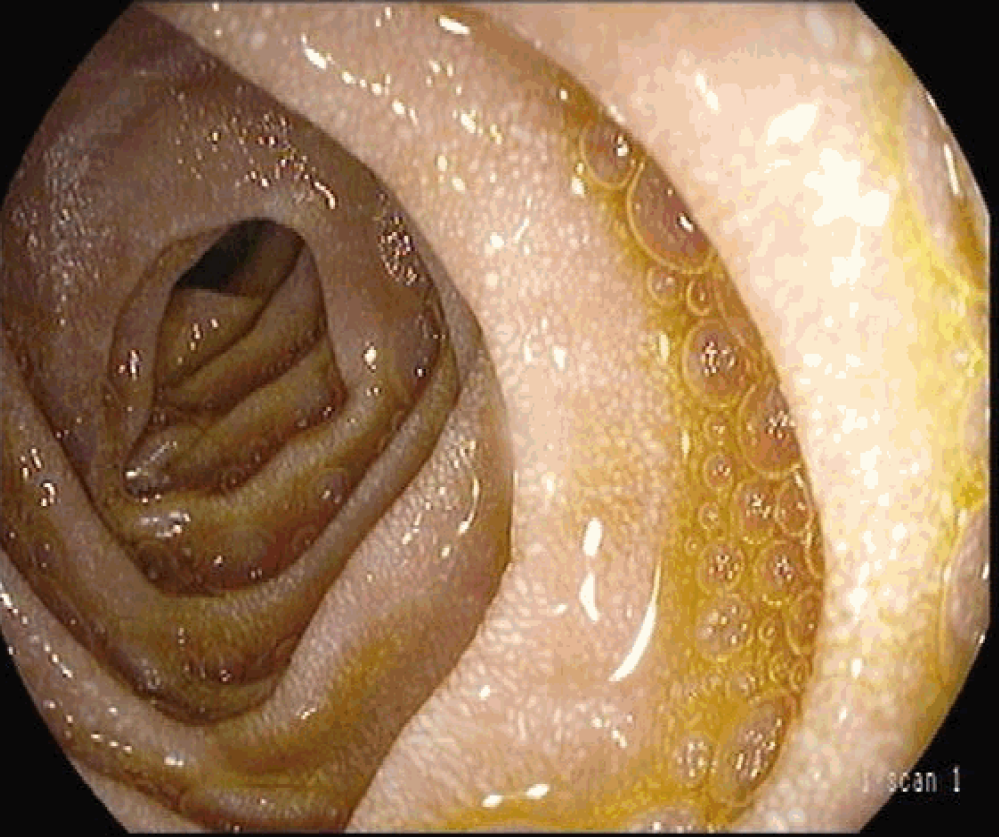
Linfangiectasias na 2ª porção do duodeno
Figura II
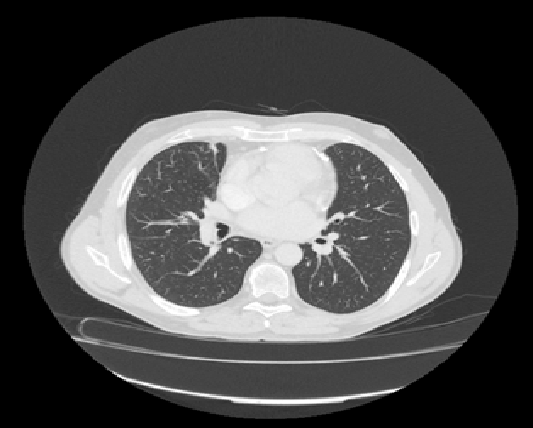
TC de tórax revelando espessamento pericárdio difuso com áreas de calcificação em placa.
Figura III
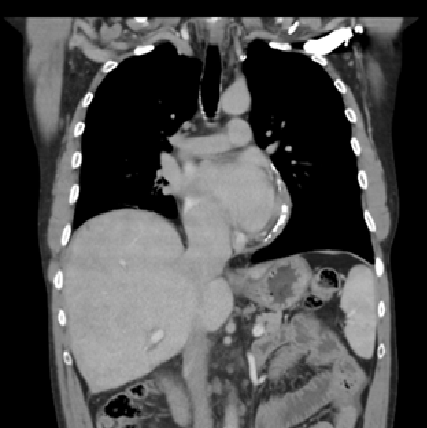
TC de tórax revelando espessamento pericárdio difuso com áreas de calcificação em placa.
Figura IV
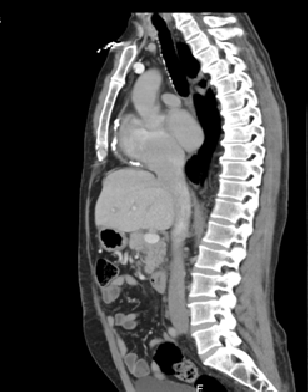
TC de tórax revelando espessamento pericárdio difuso com áreas de calcificação em placa.
Figura V
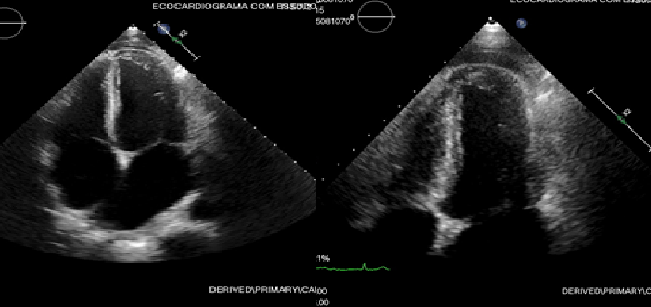
ETT: dilatação bi-auricular; ventrículo esquerdo não dilatado, alongado com septal bouncing/ ressalto do septo interventricular e interdependência ventricular
Figura VI
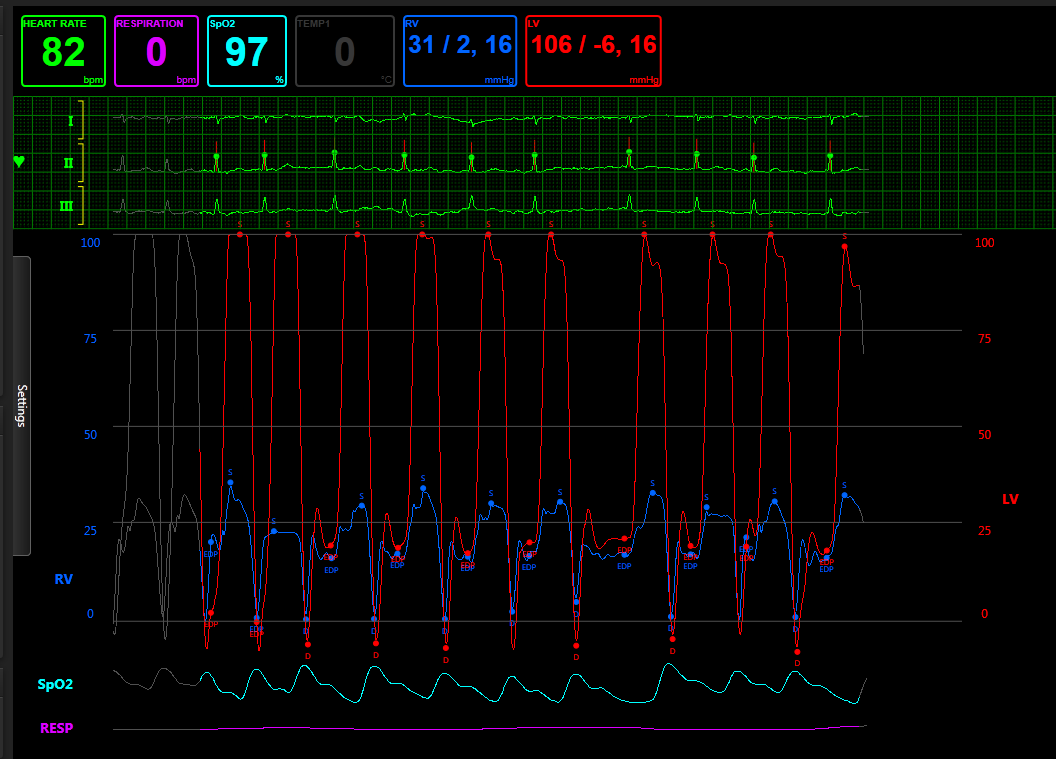
Estudo hemodinâmico: pressões ventriculares (RV: ventrículo direito e LV: ventrículo esquerdo) com equalização de pressões em diástole, com o sinal da raiz quadrada.
BIBLIOGRAFIA
1. Amiot A. Protein-losing enteropathy. Rev Med Interne. 2015;36(7):467-473
2. Moriyama H, Kohno T, Nishiyama T, et al. Images and Case Reports in Heart Failure. Published online 2011:1-3
3. Jameson JL, Kasper DL, Longo DL, Fauci AS, Hauser SL. Harrison’s Principles of Internal Medicine. 20th ed. McGraw-Hill; 2018.
4. Depboylu BC, Mootoosamy P, Vistarini N, Testuz A, El-Hamamsy I, Cikirikcioglu M. Surgical treatment of constrictive pericarditis. Ann Surg. Published online 2017:44(2): 101-6)
5. Silva D, Varela MG, Brito D, Madeira H. Cardiologia. 2012;31(10).
6. Garcia MJ. Constrictive Pericarditis Versus Restrictive Cardiomyopathy? J Am Coll Cardiol. 2016;67(17):2061-2076.
7. Meijers BKI, Schalla S, Eerens F, et al. Protein-losing enteropathy in association with constrictive pericarditis. Int J Cardiovasc Imaging. 2006;22(3-4):389-392
8. Launay D, Lambert M, Hachulla E, et al. Protein-losing enteropathy revealing an idiopathic constrictive pericarditis. Rev Med Interne. 2007;28(1):38-41







